
| Medicina | Medicina veterinara | Muzica | Psihologie | Retete | Sport |
Medicina
|
|
Qdidactic » sanatate & sport » medicina Procese fundamentale ale cineticii medicamentelor |
Procese fundamentale ale cineticii medicamentelor
PROCESE fundamentale ALE CINETICII MEDICAMENTELOR
Studiul farmacocineticii implica procese care intervin in diferite etape ale circulatiei medicamentelor in organism. Printre acestea de mare importanta sunt: trecerea prin membrane, legarea de proteinele plasmatice si transformarea biochimica a moleculelor medicamentelor.
1. TRECEREA PRIN MEMBRANE
Procesul de trecere prin membrane este implicat in absorbtia, distributia si eliminarea medicamentelor, traversarea membranelor biologice reprezentand un proces cheie limitant pentru intreg ciclul farmacocinetic.
De la absorbtie pana la eliminare, medicamentele traverseaza diferite membrane biologice ale sistemului multicompartimental al organismului, in functie de acest lucru fiecare medicament avand un profil farmacocinetic propriu.
Membranele biologice reprezinta un sistem complex semipermeabil polienzimatic, cu o grosime de 80-100 Å, care acopera celulele si organitele intracelulare, separand si controland schimburile dintre diferitele compartimente ale materiei vii. Singer si Nicolson (1972) au propus un model in care membrana are o structura in mozaic, formata din straturi lipidice bimoleculare cu proprietati fluide. Aceasta matrita fosfolipidica inglobeaza glicoproteine si lipoproteine, grupari ionice si polare proeminente pe una sau ambele fete ale membranei. Membrana poate suferi schimbari locale rapide, cu modificarea geometriei spatiale a proteinelor componente, formand canale sau pori, cu dimensiuni mai mici la nivelul membranelor celulare (8 Å) si mai mari la nivelul capilarelor (60-80 Å). Membrana celulara reprezinta si o matrice pentru enzime si farmacoreceptori.
Potentialul de trecere prin membrane este frecvent exprimat prin coeficientul de partaj lipide/apa, care este raportul concentratiei medicamentului in 2 faze nemiscibile.
Trecerea medicamentului prin membrane este dependenta de mai multi factori:
factori dependenti de membrana (continutul lipidic, starea fiziologica sau patologica a membranei, prezenta porilor, existenta unor sisteme speciale de transport, polarizarea).
factori dependenti de medicamente (masa moleculara, doza, structura chimica care determina lipo- si hidrosolubilitatea, constanta de ionizare-pKa).
factori dependenti de mediul de pe cele doua fete ale membranei (pH-ul, legarea de proteine, vascularizatia, debitul circulator local).
Transportul prin membrane implica modalitati de trecere prin membrane:
procese de transport pasiv
procese de transport specializat.
A. Procese de transport pasiv
Filtrarea sau penetrarea intervine in cazul moleculelor cu dimensiuni mici si hidrosolubile, astfel ele sunt dizolvate in apa si trec prin pori impreuna cu apa. Trecerea de pe o parte a membranei pe cealalta, determinata de diferenta de presiune hidrostatica sau osmotica si este un fenomen pasiv. Diametrul mic al porilor membranelor celulare (8Å) permite trecerea doar a moleculelor hidrosolubile mici (fiind o situatie de exceptie pentru medicamente). Moleculele mai mari pot traversa la nivelul capilarelor, care au un diametru mai mare al porilor (60-80Å) factorul limitant fiind legarea de proteinele plasmatice (macromolecule care nu trec obisnuit prin porii capilari).
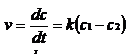
Difuziunea simpla are loc
datorita diferentei de concentratie la nivelul celor doua
fete ale membranei, deplasarea moleculelor facandu-se in sensul
gradientului de concentratie, viteza de difuziune fiind exprimata
prin legea lui Fick:
v - viteza de difuziune;
dc - diferenta de concentratie dintre cele 2 fete ale membranei;
dt - intervalul de timp in care are loc procesul de difuziune:
c1, c2 - concentratiile pe cele 2 fete ale membranei;
k - constanta de difuziune.
Capacitatea de difuziune a substantelor prin membrane este definita printr-o constanta de permeabilitate dependenta atat de proprietatile membranei, cat si de proprietatile moleculei medicamentului.
Rata transportului depinde de:
dimensiunea moleculelor;
gradul de liposolubilitate;
gradul de ionizare;
difuzibilitatea substantei
Moleculele cu dimensiuni mici difuzeaza mai repede (datorita interventiei miscarilor browniene mai active decat pentru moleculele mari)
|
Liposolubilitatea reprezinta conditia esentiala pentru traversarea membranelor lipidice, substanta medicamentoasa trebuie sa aiba un coeficient de partitie lipide/apa mare. Substantele difuzeaza cu atat mai mult cu cat sunt mai solubile in lipide, dar trebuie sa aiba si o oarecare solubilitate in apa.
Gradul de ionizare, polaritatea moleculei reprezinta de asemenea o importanta deosebita. Ionii au o solubilitate mica in grasimi deoarece in jurul sarcinilor electrice se aglomereaza dipoli de apa, de aceea moleculele ionizate au dificultate in traversarea membranelor lipidice.
De retinut este faptul ca numai moleculele nelegate de proteinele plasmatice sau tisulare si din acestea numai cele neionizate si liposolubile sunt difuzibile.
Majoritatea medicamentelor sunt electroliti slabi, solutia apoasa constand dintr-un amestec de ioni si molecule neionizate.
Capacitatea de a difuza prin membrane in cazul acizilor slabi sau a bazelor slabe este in functie de constanta de ionizare pKa proprie moleculei. Cu ajutorul acestei constante se poate calcula proportia formei ionizate in functie de diferite valori ale pH-ului folosind ecuatia Henderson- Hasselbach:
![]()
![]()
Pentru
medicamente cu caracter acid (acizi
slabi):
in care:
[AH]-reprezinta concentratia molara a formei neionizate;
[A-]- reprezinta concentratia molara a formei ionizate.
![]()
Pentru
medicamente cu caracter bazic (baze slabe):
in care :
[BH+] -reprezinta concentratia molara a formei ionizate;
[B] -reprezinta concentratia molara a formei neionizate
Cand pH=pKa, concentratiile celor doua forme (ionizata si neionizata) sunt egale(50%).
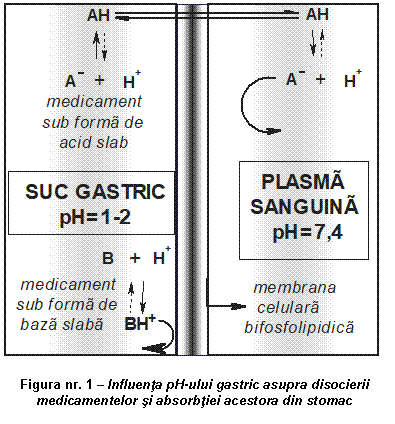
Un pH alcalin pentru medicamentele acide si un pH acid pentru medicamentele bazice, creste proportia formei ionizate, micsorand consecutiv capacitatea de trecere prin membrane. De aceea, in mediul acid din stomac se absorb bine acizii slabi, care nu sunt ionizati la acest pH, iar bazele slabe, aproape in totalitate ionizate, nu se absorb (figura nr. 1).
B. Procese de transport specializat
Unele molecule nu pot traversa membrana prin difuziune, acestea pot fi transportate prin interventia unor mecanisme specifice.
Difuziunea facilitata se face numai in sensul gradientului de concentratie si nu necesita consum de energie.
Mecanismul transportor se caracterizeaza printr-o inalta specificitate sterica, substantele transportate trebuind sa aiba o anumita structura chimica. Compusii cu structura asemanatoare pot concura pentru substratul respectiv.
Capacitatea de transport este limitata de disponibilul de molecule transportoare, existand un maxim de transport.
Transportul activ este un proces care decurge cu consum de energie in sens contrar gradientului de concentratie, necesitand prezenta unui sistem transportor si avand o inalta specificitate sterica.
Molecula substantei medicamentoase este preluata de pe o parte a membranei si este transportata pe cealalta parte. Proteina transportoare se caracterizeaza printr-un maxim de transport in unitatea de timp in functie de saturarea locurilor de legare.
Substantele cu structuri asemanatoare pot concura pentru sediile de legare ale proteinei transportoare prin competitie.
Ionii de calciu sunt transportati activ in afara celulei (impotriva gradientului de concentratie) prin ATP-aza calcica membranara (pompa de Ca2+).
ATP-aza Na+/K+-dependenta transporta ionii de sodiu in afara celulei (in stare de repaus) prin schimb cu ionii de potasiu pe baza energiei furnizate de ATP.
Ionii de I- din plasma sanguina sunt concentrati cu precadere la nivelul glandei tiroide printr-un mecanism de transport activ. De asemenea, patrunderea unor aminoacizi si hexoze (glucoza) la nivelul sistemului nervos central prin traversarea membranei hemato-encefalice se face prin transport activ.
Anumite conditii sau chiar anumiti compusi chimici (inhibitori metabolici) pot incetini sau chiar bloca procesul de transport activ prin inhibarea formarii de energie necesara (ceea ce denota dependenta acestui proces de integritatea mecanismelor celulare de producere a energiei, care alimenteaza procesele de formare a complexelor substanta - transportor (purtator).
Sistemele de trasport activ cu specificitate redusa intervin in transferul unor acizi si baze din plasma in tubii renali, influentand excretia unor medicamente (de exemplu, penicilina).
Astfel de sisteme intervin si in secretia biliara a medicamentelor.
Transportul prin ioni pereche
Reprezinta o modalitate de a traversa membranele, de catre unii compusi puternic ionizati (acizi sulfonici, saruri cuaternare de amoniu) si explica absorbtia din tubul digestiv in cantitati mici a acestor substate .
Complecsi de tip ioni-pereche pot forma unele medicamente puternic hidrofile cu unii compusi endogeni (de exemplu mucina din lumenul intestinal) care in felul acesta traverseaza membrana lipidica prin difuziune.
Pinocitoza este tot o modalitate de transport si consta in inglobarea de catre celule a unor picaturi care contin substata dizolvata. Picatura este inconjurata de o portiune de membrana formand o vezicula, care apoi se detaseaza in citoplasma. Acest tip de transport se intalneste in cazul lipidelor, vitamine liposolubile (A, D, E, K).
Unele medicamente pot fi absorbite prin mai multe mecanisme: de exemplu glicozidele tonicardiace se absorb partial prin difuziune pasiva, partial prin transport activ.
La nivelul diferitelor organe si tesuturi sunt disponibile mai multe mecanisme de transport. Astfel in cavitatea bucala predomina difuziunea si filtrarea; in stomac difuziunea pasiva; in intestinul subtire toate tipurile de transport; in intestinul gros si rect difuziunea, filtrarea si pinocitoza; la nivelul tegumentelor difuziunea si filtrarea (pentru molecule mici).
II. 1.2. LEGAREA DE PROTEINELE PLASMATICE
Majoritatea medicamentelor circula in sange sub doua forme: molecule libere (dizolvate in plasma) si molecule legate de proteinele plasmatice. Aceste proteine care au capacitate de legare atat pentru medicamente, cat si pentru unele substante endogene sunt: albuminele serice, alfa1-acid glicoproteina, lipoproteinele.
Albuminele plasmatice reprezinta aproximativ 50% din proteinele serice, ele prezentand minimum 6 situsuri de legare. Exista locuri de legare specifice acizilor grasi si bilirubinei, dar si 2 pozitii specifice de legare pentru medicamente, mai ales pentru cele cu caracter acid, care sunt intens ionizate la pH-ul plasmatic (pH=7,4). De aceea, fixarea de albumine se face adesea prin legaturi ionice. Medicamentele cu caracter bazic, precum si cele neionizate beneficiaza de mai multe situsuri de legare, nespecifice, dar legaturile formate sunt slabe (forte Van der Waals, punti de hidrogen).
Alfa 1- acid glicoproteina leaga cu precadere molecule de medicament cu caracter bazic.
Medicamentele se leaga de proteinele plasmatice formand un complex medicament-proteina conform legii actiunii maselor :
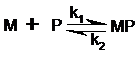
unde simbolurile reprezinta:
M -moleculele libere de medicament;
P -moleculele de proteina;
MP -complex format medicament-proteina;
k1 - constanta de asociere;
k2 - constanta de disociere.
Aceasta reactie e reversibila existand un echilibru dinamic intre cele 2 forme.
Legarea medicamentului de proteine se face de regula prin legaturi polare (punti de hidrogen, forte van der Waals), foarte rar intervin legaturi covalente, stabile.
Ea se caracterizeaza prin doi parametri:
-afinitatea;
-procentul de fixare.
![]()
Afinitatea care se exprima printr-o constanta Ka
reprezentand raportul dintre constantele vitezei de asociatie si
disociatie a complexului medicament-proteina:
unde:
k1 - constanta de asociere;
k2 - constanta de disociere;
![]()
Procentul de fixare reprezinta raportul
dintre fractia libera si cantitatea totala de medicament
din plasma, conform formulei:
fn= fractia nelegata
Forma legata (de proteinele plasmatice) - este inactiva, deoarece moleculele de medicament in aceasta forma nu vor putea trece prin membrane (forma legata nu poate difuza in tesuturi, nu poate filtra glomerular, deci influenteaza distributia medicamentului in organism).
Albuminele serice scad in boli hepatice si renale. La astfel de bolnavi, capacitatea de legare a medicamentului scade, rezultand cresterea actiunilor farmacodinamice si adverse. In uremie (uree > 200 mg %, insuficienta renala stadiul IV) este scazuta capacitatea de legare a unor medicamente acide (salicilati, barbiturice, sulfamide).
La administrarea mai multor medicamente in procesul de legare de proteinele plasmatice, acestea pot intra in competitie pentru acelasi loc de legare, avand loc 'interactiuni de deplasare'.
Acest fenomen se intalneste mai ales la substantele cu caracter acid, ionizate la pH ul sanguin si care se leaga in proportie mare de albumine (fenilbutazona, anticoagulantele cumarinice, acidul nalidixic, antidiabeticele). Medicamentele slab acide pot intra in competitie, pentru sediile de legare de proteine, cu moleculele endogene de acelasi tip. Astfel, sulfamidele si fenilbutazona pot deplasa bilirubina de pe albumine, crescand concentratia de bilirubina libera pana la un potential neurotoxic pentru nou nascut (icter nuclear). Aceste aspecte sunt importante pentru practica terapeutica, deoarece nivelul fractiei nelegate poate creste mult, determinand in mod corespunzator cresterea efectelor farmacodinamice si farmacotoxicologice.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2026 - Toate drepturile rezervate -| |
|
|
|||
|
|||
|
|||
Referate pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








