
| Medicina | Medicina veterinara | Muzica | Psihologie | Retete | Sport |
Medicina
|
|
Qdidactic » sanatate & sport » medicina Implicarea celulelor stem in ingineria tisulara - cardiomioplastia tisulara |
Implicarea celulelor stem in ingineria tisulara - cardiomioplastia tisulara
Implicarea celulelor stem in ingineria tisulara - cardiomioplastia tisulara
Multe forme de afectiuni cardiace sunt caracterizate prin pierderea progresiva a cardiomiocitelor (apoptoza sau necroza) ducand progresiv la scaderea capacitatii de adaptare si moarte. Hipertrofia miocitelor este singura cale de compensare a pierderii numarului mare de celule, fiind singura modalitate de raspuns a cordului la factorii insultanti.
Regenerari cardiace a fost descrise la pestele zebra dupa rezectie ventriculara, la soareci MRL dupa criolezare, comparativ cu cordul uman care are mecanisme inadecvate pentru a induce regenerarea cardiaca. Studii recente au relevat prezenta de celule stem cardiace si capacitatea lor limitata de regenerare. De aceea transplantarea celulara este o noua cale de a creste capacitatea limitata de regenerare a cordului lezat. Studii recente de transplant celular indica formarea de cardiomiocite si alte tipuri celulare dupa transplantul de celule stem din maduva hematogena, celule stem cardiace, celule stem embrionare (ES) sau migrarea de celule precursoare la locul lezat. Transplantul celular este un mijloc de tratament foarte important pentru a induce regenerarea miocardului cu distructii celulare (Satin, J., 2004).
Recent multiple tipuri de celule transplantate incluzand si celulele stem embrionare pluripotente (Fig.33) au determinat succese semnificative in reluarea functiei miocardului lezat. Cu toate acestea raman de identificat tipurile celulare optime de celula, tehnica lor de cultivare si diferentiere precum si modalitatea de grefare a acestora.
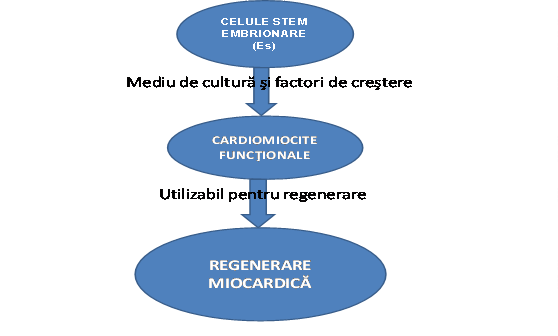
Fig.nr.10 - Protocolul de utilizare a celulelor stem embrionare
Izolarea si cultivarea celulelor stem embrionare pluripotente inseamna un nou instrument pentru medicina regenerativa si pentru terapia bolilor cardiovasculare. Capacitatea de diferentiere in vitro a celulelor ES in diferite tipuri celulare prezente in organismul adult a insemnat un instrument perfect pentru diferite arii de cercetare (Robert L., si col 2004).
Celulele stem embrionare, celulele stem hematopoetice, mezenchimale, celule stem stromale si alte tipuri celulare necaracterizate inca pana astazi sunt surse majore utilizabile in terapia celulara (Fig. 10) (Sophie Lev si col., 2005).
Inainte de demersurile clinice populatia celulara prelevata se caracterizeaza prin observarea prezentei markerilor specifici de suprafata. Pe langa celulele stem embrionare, cele provenite din maduva ososa reprezinta o sursa alternativa foarte importanta pentru transplant. Numeroase populatii mononucleare din maduva osoasa au fost izolate pe baza markerilor specifici CD34+ si prezenta markerului de linie (lin) un antigen prezent in celule (Mauro K. si col., 2006).
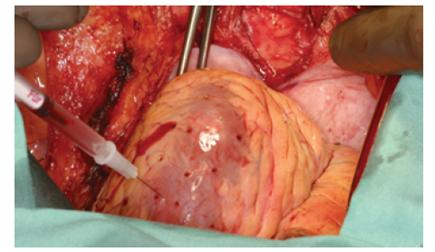
Fig.nr.11- Injectarea intramiocardica de celule stem
www.touchcardiology.com
|
Celulele stem mezenchimale din maduva ososasa pot fi selectate prin aderenta lor la placa de cultura, o proprietate pe care celulele hematopoetice sau alte celule nu poseda. Celulele stem mezenchimale sunt CD 34 -, c-kit - si CD45- acesta din urma fiind un marker panleucocitar.
Numeroase populatii de celule stem din maduva osoasa sunt capabile sa-si limiteze cresterea si sa incapa dezvoltarea spre celule cardiomiocitare. Multe populatii au fost testate pe numeroase modele umane sau animale evaluand potentialul lor cardiomioplastic. Celulele specifice cardiace, au contractii spontane cu structuri asemanatoare cardiomiocitelor. Aceste celule derivate din celule stromale medulare dupa expunerea cu cinci azacitidine se comporta asemanator sinusului nodal si celulelor ventriculare.
Studii recente pe celule cardiace derivate din maduva ososasa umana utilizand mediu de cultura netoxic, constituie modelutilizabil pe scara larga in producerea de celule pentru transplant. Celulele hematopoetice din maduva ososasa sunt utilizate pe scara larga in caz de infarct. A fost demonstrat ca injectarea intramiocardica de celule lin- si c-kit+ la soareci induce regenerarea miocardica. Celulele injectate local induc formarea de miocite noi, celule endoteliale si celule musculare netede. Aceste celule exprima connexin 43, o proteina gap junction la celulele cardiace, responsabila pentru cuplarea intercelulara.
Expresia connexinei 43 demonstreaza o semnificativa interactiune functionala intre celulele locale cardiace. Pe langa celule mezenchimale si celule stem hematopoetice si alte populatii celulare progenitoare au fost descoperite in maduva ososasa. Multe studii utilizeaza populatii heteroloage mononucleare de celule stem din maduva osoasa, ca model pentru cardioplastia celulara.
In particular celulele mononucleare si cele stem embrionare derivate din maduva osoasa prezinta capacitata de a se diferentia spre celule cardiace functionale fapt demonstrat pe modele animal si oameni. Inca este neclar ce tipuri celulare din aceasta populatie ar fi responsabile de ameliorarea functiei cardiace. Datorita avantajului dat de populatia celulara foarte heteroloaga aceste celule au abilitatea de a fi transplantate, avand capacitatea de a se diferentia in celule endoteliale, miocite, celule vasculare si contribuind astfel la ameliorarea functiei cardiace (Reppel M., si col. 2004).
Mioblastii scheletici sau celulele satelite sunt celule precursoare a muschilor scheletici. Grefa de mioblasti scheletici se transforma dupa implantare in miotubuli striati in interiorul cicatricei. Desi nu se observa clasica sincronizare celula-celula, miofibrilele se pot observa aliniat in paralel cu fibrele musculare. Aceste studii demonstreaza viabilitatea tisulara, contractibilitatea si reducerea dilatarii cavitatii ventriculare la pacientii la care s-a facut transplantul.
Deoarece toate aceste transplante se efectueaza simultan cu bypass-ul in ventricolul stang, este dificil de stabilit daca ameliorarea functiei cardiace este dat de revascularizare sau de terapia celulara. Avantajul utilizarii mioblastior scheletici este dat de faptul ca aceste celule rezista la ischemie si au capacitate de a prolifera usor (Wobus A., si col. 2005).
Cardiomiocite fetale FMCs. Celulele cardiace fetale sunt ideale pentru terapia celulara. S-au obtinut transplante de celule cardiace fetale direct in miocardul de soareci rezultand astfel ameliorarea functiei cardiace. Studii recente au demonstrat prezenta de discuri intercalate si conexiuni intercelulare fara jonctiuni gap, intre celulele grefate si cele locale. Alte studii arata supravietuirea timp de 6 saptamani dupa transplant ameliorare rejectarii si reducerea la minim a dischineziei in regiunea cu infarct (Fig. 12).
Celulele cardiace fetale mioblastice injectate concomitent intramiocardic, in caz de infarct miocardic atrial, demonstreaza o ameliorare a functiei cardiace. Consideratiile etice reprezinta bariera primara a cercetarilor in cazul cardiomiocitelor fetale umane .

Fig.nr .12 - Inducerea experimentala a infarctlui miocardic si aplicare
tratamentul prin inginerie tisulara (www.cardiacmatters.co)
Celule stem cardiace adulte Asc. Reprezinta un alt tip de celule atractive pentru cardiomioplastie. Existenta celulelelor stem cardiace a fost pusa sub semnul intrebarii si totusi studii recente demonstreaza identificarea la soareci adulti de celule stem cardiace adult, Sca 1 +. Intr-un model de ischemie/ reperfuzie, aceste celule stem cardiace au fost injectate intravascular, localizandu-se dupa injectare la nivelul miocardului afectat.
Analiza postmortem a cordului uman cu stenoza si cu megalia masei cardiace, releva existenta de celule progenitoare cardiace si miocitare, aceste celule fiind pozitive pentru antigene de suprafata detectate la celulele primitive. Celulele stem cardiace adulte au fost utilizate in terapia infarctului miocardic.
Celulele stem cardiace exogene izolate de la sobolani si injectate intravascular in studii de ischemie/reperfuzie stopeaza remodelarea si amelioreaza functia ventricolului stang (Reppel M., si col. 2004).
Celulele progenitoare endoteliale EPCs
Aceste celule sunt prezente in maduva osoasa, numarul de celule progenitoare endoteliale circulante fiind corelat cu activitatea sistemului cardiovascular. Receptorul KDR este un factor de crestere receptor tirozin kinaza (Kinase insert domain receptor) si poate fi identificat in celulele progenitoare endoteliale din maduva ososasa.
Celulele progenitorii endoteliale se definesc ca receptor: CD34+ si factori de crestere receptor tirozin kinaza (KDR+) aratand progresia aterosclerozei si moartea din cauze cardiace. Celulele endoteliale progenitoare au un risc potential de stratificare. Factorul stimulator de colonii granulocitare (G-CSF) este utilizat pentru a mobiliza receptorul CD34+ din sangele periferic. Examenele clinice Magic cell si Phase II sunt teste in care este utilizat factorul stimulator de colonii granulocitare (G-CSF). La pacienti cu infarct miocardic atrial, cu implant metalic, ce prezinta leziuni miocardice, celulele CD34+ sunt mobilizate cu factorul stimulator de colonii granulocitare G-CSF, fiind colectate si reintroduse prin infuzie intracoronariana. Terapia cu celule provenind din coloniile granulocitare si terapia cu celule stem din sangele periferic amelioreaza functia cardiaca, cu toate acestea fiind observat o rata mare de restenozare la pacienti tratati cu factor stimulator de colonii granulocitare (G-CSF) fata de control (Reppel M., si col. 2004).
Rezultatele preliminare demonstreaza ca perfuzia intracoronara cu celule stem mobilizate cu ajutorul factorului stimulator de colonii granulocitare din sangele periferic este asociata cu marirea ejectiei fractiuni implantate in ventricolul stang (Shengkun S. si col., 2003).
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
|
|||
Lucrari pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








