
| Medicina | Medicina veterinara | Muzica | Psihologie | Retete | Sport |
Medicina
|
|
Qdidactic » sanatate & sport » medicina Cancerul mamar - epidemiologie, factorii de risc in cancerul de san, semnele si simptomele cancerului de san |
Cancerul mamar - epidemiologie, factorii de risc in cancerul de san, semnele si simptomele cancerului de san
Cancerul mamar
1. Epidemiologie
Cancerul de san nu este o boalǎ a societǎtii moderne, ea era cunoscutǎ incǎ din Egiptul antic 1600 i.e.n. Cancerul de san a devenit o problemǎ majorǎ de sǎnǎtate in ultimii 50 de ani, afectand aproximativ una din opt femei in timpul vietii. Cu aproximativ 1.000.000 cazuri noi si 400.000 decese la nivel mondial in fiecare an, cancerul de san este cea mai comunǎ formǎ de manifestare malignǎ la femei si reprezintǎ aproximativ 18% din totalitatea cancerelor la aceastǎ grupǎ populationalǎ, fiind totodatǎ principala cauzǎ de deces oncologic la femei.
Incidenta bolii este in crestere, atat in tǎrile industrializate, cat si in tǎrile in curs de dezvoltare. In SUA, incidenta bolii a crescut cu 1-2% pe an incepand din 1960. In Romania se inregistreazǎ aproximativ 6400 de cazuri noi anual.(57)
2. Factorii de risc in cancerul de san
Ceea ce se cunoaste actualmente despre factorii de risc ai cancerului mamar se referǎ la factori de risc care nu pot fi influentati si factori de risc si stil de viatǎ care pot fi modificati.
2.1. Factorii de risc ce nu pot fi modificati:
2.1.1. Factori anamnestici
sexul: simplul fapt de a fi femeie reprezintǎ un risc constant pentru cancerul de san. Barbatii pot face cancer mamar, dar acesta este mult mai rar.
varsta inaintatǎ (>60 de ani): varsta este cel mai important factor de risc pentru dezvoltarea cancerului de san, riscul crescand cu varsta
factori menstruali: menarha la o varsta micǎ (inaintea varstei de 12 ani), menopauza tardivǎ (peste 50 ani), varsta inaintatǎ la prima nastere (peste 30 ani) sau nuliparitatea, pot creste riscul de aparitie a cancerului de san prin modificarea expunerii de-a lungul vietii la actiunea hormonilor.(55)
2.1.2. Factori genetici:
rasa alba: femeile acestei rase prezintǎ un risc mai mare de a dezvolta cancer de san decat femeile de culoare, dar acestea din urmǎ au o ratǎ mai mare a mortalitǎtii in caz de cancer. Femeile asiatice si hispanice, dupǎ cum se aratǎ in studiile nord-americane, au un risc mai mic pentru cancerul mamar.
istoricul familial de cancer mamar poate fi asociat cu o crestere a riscului: istoricul de cancer de san la o ruda de gradul I de sex feminin (mama, sora sau fiica) este asociat cu riscul cel mai crescut, in special cand ruda a fost diagnosticatǎ la o varsta tanarǎ
istoricul personal de cancer de san: un istoric de cancer mamar invaziv sau in situ creste riscul de aparitie/dezvoltare a unui nou cancer in tesutul mamar restant in fiecare san cu 0,5 - 1% pe an. De asemenea, o femeie cu un cancer la un san are "sanse" mai mari de a dezvolta un cancer si la sanul celǎlalt, acesta putand fi diferit de recurenta de la primul.
sindromul Lynch(57)
alterǎri ale genelor BRCA-1 si BRCA2: cancerul de san ereditar apare la varste tinere; probabil este bilateral si adesea apare la mai multi membrii ai unei familii de-a lungul a 3 sau 4 generatii, incluzand si femeile din latura paternǎ a familiei. Se considerǎ cǎ aproximativ 5-10% din cancerele de san sunt mostenite. In 1994 au fost izolate douǎ gene ale susceptibilitǎtii pentru cancerul de san, BRCA1 si BRCA2. Se apreciazǎ cǎ impreunǎ sunt rǎspunzǎtoare de aparitia a 40-50% din cancerele de san ereditare. Fiecare dintre cele peste 200 mutatii posibile poartǎ un risc diferit de dezvoltare a bolii si riscul poate fi modificat de alte gene, de stilul de viatǎ sau de factorii de mediu. In prezent, se poate estima procentajul purtǎtorilor care vor dezvolta cancer de san, mai putin decat riscul individual al unei femei. Prevalenta estimatǎ pentru BRCA1 in populatia generalǎ variazǎ intre 0,04% si 0,2%. Astfel, se poate calcula pentru anumite populatii cu risc prevalenta mutatiilor genelor BRCA1 si BRCA2.
2.1. Factori anatomici: - tesut mamar dens
2.1.4. Factori histologici: - hiperplazia epitelialǎ atipicǎ sau alte afectiuni benigne ale sanului in antecedentele personale
2.1.5. Factori hormonali: - expunerea la estrogeni
2.1.6. Expunerea la toxice: - expunerea la radiatii; femeile care au avut in copilǎrie sau la o varstǎ tanǎrǎ tratament radiologic (radioterapie) la nivelul toracelui au un risc crescut pentru cancer.
2.2. Factori de risc care pot fi influentati si care tin de stilul de viatǎ si obiceiuri
2.2.1. Factori anamnestici:
lipsa alaptǎrii la san: anumite studii au arǎtat cǎ alǎptarea copilului la ambii sani panǎ la varsta de 1,5-2 ani poate scǎdea riscul aparitiei cancerului mamar.
inducerea avortului: desi unele studii au sugerat ca un avort indus in antecedente poate spori riscul de cancer mamar, alte studii nu au evidentiat aceastǎ asociere. Datele din literatura de specialitate si un studiu prospectiv recent sugereazǎ cǎ riscul pentru cancerul mamar probabil nu este corelat cu inducerea avortului. Deci nu existǎ o legǎturǎ directǎ intre avort si cancerul mamar. (55)
2.2.2.Factori hormonali:
utilizarea pilulelor contraceptive: ramane incǎ neclar rolul pilulelor contraceptive ca factor de risc pentru cancerul de san. Totusi, femeile care au oprit folosirea contraceptivelor orale cu cel putin 10 ani in urmǎ, au acelasi risc ca si cele care nu au folosit niciodatǎ contraceptive orale.
terapia de substituire cu estrogeni (ERT): folosirea pe termen lung, peste 10 ani, a tratamentului cu hormoni estrogeni (numitǎ si terapie de substituire), pentru a atenua efectele secundare ale menopauzei, poate sǎ inducǎ o crestere usoarǎ a riscului pentru cancerul de san. Desi beneficiile ERT sunt numeroase, incluzand un risc scǎzut pentru afectiunile cardiovasculare si osteoporoza, este necesarǎ o cercetare intensǎ pentru a imbunǎtǎti intelegerea relatei dintre ERT si cancerul mamar, atat in beneficiul femeilor care nu au avut cancer mamar, cat si al celor tratate pentru aceasta boalǎ.
2.2.Modul de viatǎ:
exercitiile fizice: activitatea fizicǎ poate modifica nivelurile hormonilor naturali care afecteazǎ tesutul mamar si astfel reduce riscul de aparitie a cancerului de san.
dieta: relatia dintre dietǎ si riscul pentru cancerul de san se aflǎ incǎ in stadiul de cercetare, deoarece datele actuale publicate sunt controversate. Este posibil sǎ existe o legaturǎ intre obezitate si riscul de cancer mamar, in special pentru femeile aflate la menopauzǎ. Legatura dintre greutatea corporalǎ si cancerul de san este foarte complexǎ. De exemplu, se stie cǎ riscul este mai ridicat pentru femeile care au crescut in greutate fiind adulte, dar nu si pentru acelea care au fost supraponderale incǎ din copilǎrie.
|
consumul de alcool: literatura de specialitate sugereazǎ cǎ ingestia de alcool poate fi corelatǎ cu o usoara crestere a riscului de aparitie a cancerului de san. In prezent, mecanismul biologic care ar putea explica asocierea consumului de alcool si riscul pentru cancerul de san nu este cunoscut, desi unele studii clinice sugereazǎ cǎ alcoolul ar putea creste nivelurile estrogenilor circulanti. Femeile care consumǎ zilnic o bǎuturǎ alcoolicǎ au o crestere micǎ a riscului, spre deosebire de cele care consumǎ douǎ panǎ la cinci portii de bǎuturi alcoolice, la care riscul creste de 1,5 ori fatǎ de cele care nu consumǎ alcool.
2.2.4. Expunerea la toxice:
expunerea la pesticide: precum DDT, a fost privitǎ cu o atentie crescandǎ de cǎtre cercetǎtori, deoarece unele pesticide pot fi estrogeni, astfel incat pot mima activitatea estrogenilor naturali.
expunerea la doze mari de radiatii ionizante
2.Factori care nu influenteazǎ riscul pentru cancerul de san:
1. Fumatul: nu a fost incǎ demonstratǎ o legǎturǎ directǎ intre fumat si riscul pentru cancer de san, desi fumatul reprezintǎ un factor de risc important pentru bolile cardiovasculare si pentru cancerul bronho-pulmonar. (57)
2. Mediul inconjurǎtor: cercetǎrile actuale nu au arǎtat o legaturǎ clarǎ intre riscul pentru cancerul mamar si expunerea la poluanti.
Antiperspirantele: desi internetul a creat rumoare prin lansarea ideii cǎ antiperspirantele ar reprezenta un factor de risc pentru cancerul mamar prin impiedicarea circulatiei limfatice din axilǎ, nu s-au gǎsit dovezile stiintifice care sǎ sprijine aceastǎ idee.
Semnele si simptomele cancerului de san
Cel mai comun semn de cancer de san este aparitia unui nodul sau a unei tumori noi in san. Cand aceasta este nedureroasǎ, durǎ si neregulatǎ, este foarte probabil sǎ fie cancer. Dar tumorile canceroase pot fi si rotunde, elastice si regulate. Existǎ totusi, in proportie de panǎ la 10% si paciente care au durere in san, dar fǎrǎ o masǎ tumoralǎ palpabilǎ. Este important ca atunci cand apare ceva neobisnuit in san, pacientul trebuie sǎ se adreseze imediat medicului.
Alte semne ale cancerului de san pot fi:
modificǎrile persistente ale sanului, precum: ingrosarea tegumentului, tumefactia unei pǎrti a sanului, iritatia sau retractia tegumentului, ulceratia sanului;
durerea la nivelul mamelonului sau retractia acestuia;
eritemul, scarificarea sau eczematizarea mamelonului;
scurgerile sau secretiile mamelonare, diferite de laptele matern;
adenopatia axilarǎ uni- sau bilateralǎ;
adenopatia supraclavicularǎ;
edemul bratului.(55)
4. Screeningul cancerului de san
Societatea Americanǎ de Cancer recomandǎ pentru depistarea cancerului de san, la femeile asimptomatice, urmǎtoarele:
varsta de 20-39 ani: autoexaminare lunarǎ a sanilor, examen clinic al sanului la fiecare 3 ani;
varsta de 40 ani: autoexaminare lunarǎ a sanilor, examen clinic al sanului si mamografie anuale.
Din punct de vedere istoric, dovezile stiintifice care sprijinǎ screening-ul cancerului mamar de rutinǎ au fost mai puternice pentru femeile cu varsta de peste 50 ani, decat pentru cele de 40 ani.(63)
Screening-ul prin mamografii regulate a redus mortalitatea prin neoplasm de san cu cel putin 30% la femeile de 50 ani sau mai in varstǎ. Totusi, interpretarea rezultatelor pentru reducerea mortalitǎtii la femeile cu varsta intre 40 si 49 ani a fost un subiect mult controversat. O datǎ cu prelungirea duratei de supraveghere, dovezile unui beneficiu pentru femeile de 40 - 49 ani au devenit apropiate de cele observate la femeile cu varsta de peste 50 ani.
Tot in SUA, institutul National de Cancer Bethesda(54) face urmǎtoarele recomandǎri:
femeile cu varsta de 40 ani sau mai mult ar trebui supuse unei mamografii de screening la fiecare 2 ani;
femeile cu risc inalt pentru cancerul de san ar trebui sǎ cearǎ sfatul specialistilor atat in ceea ce priveste necesitatea efectuǎrii mamografiilor de screening inainte de varsta de 40 ani, cat si frecventa screening-ului.
La noi in tara, institutul Oncologic recomandǎ prin cabinetele de preventie:
pentru femeile de 40-45 ani, autoexaminarea lunarǎ a sanilor, examinarea clinicǎ anualǎ a sanilor si mamografia la 3 ani;
pentru femeile de 45-50 ani, autoexaminarea lunarǎ a sanilor, controlul anual de cǎtre medic si efectuarea unei mamografii de screening la fiecare 2 ani.
pentru femeile peste 50 ani, autoexaminarea lunarǎ, examinarea anualǎ de cǎtre medic si mamografii anuale.(57, 55)
5. Stadializarea cancerului de san
Stadializarea este o metodǎ de cuantificare care a fost dezvoltatǎ pentru a descrie extinderea cancerului. Pentru stadializarea cancerului de san pot fi efectuate mai multe manopere medicale printre care: examinarea clinicǎ a sanului, radiografie toracicǎ, mamografie, tomografie computerizatǎ, rezonantǎ magneticǎ nuclearǎ, teste serologice, biopsie. Stadializarea ajutǎ clinicianul sǎ aprecieze durata de viatǎ, riscul de recurentǎ si, de asemenea, il ajutǎ sǎ planifice tratamentul. In general, cu cat e mai mic stadiul, cu atat prognosticul persoanei e mai bun.
5.1. Clasificarea histologicǎ
Cancerul de san este clasificat intr-o varietate de tipuri histologice, unele dintre ele avand importantǎ in prognostic. De exemplu, printre tipurile histologice favorabile se includ: tipul mucinos, medular si carcinom cu celule cilindrice.
Cancerul ductal invaziv sau infiltrativ este cea mai comunǎ formǎ histologicǎ de cancer mamar apǎrand in aproximativ 70-80% din cazuri.
Carcinom nediferentiat
Carcinom ductal : -intraductal in situ
-invaziv cu componentǎ intraductalǎ
-invaziv nespecific
-comedo
-inflamator
-medular cu infiltrate limfoide
-mucinos (coloid)
-papilar
-schiros
-tubular
-alte tipuri
Carcinom lobular:-in situ
-invaziv cu componentǎ predominantǎ in situ
-invaziv (57)
Tipuri celulare ce afecteazǎ mamelonul: - boala Paget nespecificǎ
boala Paget asociatǎ cu carcinom intraductal
boala Paget asociatǎ cu carcinom invaziv ductal
Carcinoame nespecifice
Alte tumori care afecteazǎ sanul, dar nu sunt considerate cancere mamare tipice:
- cystosarcoma phyllodes
- angiosarcomul
- limfomul primar
5.2 Sistemul TNM
Anatomopatologii au un sistem specific de stadializare al cancerului, cunoscut ca si sistemul TNM (T=mǎrimea tumorii, N=noduli palpabili, M=metastaze), sistem care a fost conceput de American Joint Committee on Cancer (AJCC) in colaborare cu National Cancer Institute (NCI).(54)
In cadrul sistemulul TNM, litera T urmatǎ de cifre de la 0 la 4 se referǎ la dimensiunea tumorii primare si la diseminarea acesteia spre piele si peretele toracic subiacent sanului. Cu cat numǎrul asociat literei T este mai mare, cu atat tumora este mai extinsǎ in tesuturile din jurul sanului.
Tx: tumora primarǎ nu poate fi pusǎ in evidentǎ
T0: tumorǎ nepalpabilǎ
Tis: carcinom in situ: carcinom lobular in situ (LCIS), carcinom ductal in situ (DCIS) sau boala Paget fǎrǎ o masǎ tumoralǎ palpabilǎ
T1: existenta unei tumori mai micǎ de 2 cm in diametru
T1 mic: microinvazie tumorǎ mai micǎ decat 0.1cm
T1a: tumorǎ cuprinsǎ intre 0.1-0.5 cm
T1b: tumorǎ cuprinsǎ intre 0.5- 1cm
T1c: tumorǎ cuprinsǎ intre 1-2 cm
T2: existenta unei tumori cuprinse intre 2 si 5 cm in diametru
T3: existenta unei tumori mai mari de 5 cm in diametru
T4: existenta unei tumori de orice mǎrime cu extindere directǎ la peretele toracic, nodulii limfatici pectorali si la tegument, incluzand aici carcinomul inflamator si modificǎrile texturii tegumentare ale sanului (ulceratii).
T4a: extinderea la peretele toracic fǎrǎ a include muschiul pectoral
T4b: edem (inclusiv coaja de portocalǎ) sau ulceratii ale pielii sanului sau noduli de permeatie limitati la nivelul tegumentului sanului
T4c: T4a + T4b
T4d: carcinomul inflamator (caracterizat prin induratie difuzǎ a pielii de aspect erizipeloid, in mod obisnuit fǎrǎ masǎ palpabila)(57)
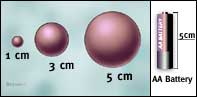 Fig.4 Dimensiunea
comparativǎ a tumorilor co o
baterie AA
Fig.4 Dimensiunea
comparativǎ a tumorilor co o
baterie AA
Litera N, urmatǎ de cifre de la 0 la 3 se referǎ la extinderea cǎtre nodulii limfatici regionali si in cazul afectǎrii lor, dacǎ acestia sunt fixati de alte structuri de sub axilǎ.
Nx: nodulii limfatici regionali nu pot fi evaluati (au fost excizati anterior,etc)
N0: nodulii limfatici regionali nu se palpeazǎ
N1: metastaze in nodulii limfatici axilari homolaterali mobili
N2: metastaze in nodulii limfatici axilari homolaterali fixati intre ei sau metastaze clinic aparente in nodulii mamari interni homolaterali in absenta metastazelor clinic evidente in nodulii limfatici axilari homolaterali
N2a: metastaze in nodulii limfatici axilari homolaterali fixati intre ei sau cu alte structuri
N2b: metastaze clinic aparente in nodulii mamari interni homolaterali si in absenta metastazelor clinic aparente in nodulii limfatici axilari homolaterali
N3: metastaze in nodulii limfatici infraclaviculari homolaterali cu sau fǎrǎ afectarea nodulilor limfatici axilari; sau noduli limfatici mamari interni cu metastaze clinic aparente in prezenta metastazelor evidente in nodulii limfatici axilari; sau metastaze in nodulii limfatici supraclaviculari cu sau fǎrǎ afectarea nodulilor limfatici mamari interni
N3a: metastaze in nodulii infraclaviculari homolaterali
N3b: metastaze in nodulii limfatici mamari interni si axilari
N3c: metastaze in nodulii limfatici supraclaviculari homolaterali
Litera M, urmatǎ de cifre de la 0 la 1 indicǎ existenta metastazelor in organele invecinate (plǎmani, oase) sau in nodulii limfatici
Mx: metastazele la distantǎ nu pot fi evidentiate
M0: nu existǎ metastaze in alte organe
M1: existǎ metastaze in organele invecinate
5.3 Clasificarea patologicǎ pTNM
pT- categoriile pT corespund categoriilor de T
pN-clasificarea patologicǎ necesitǎ rezectia si examinarea ganglionilor limfatici din statia I; o astfel de rezectie implicǎ in mod normal 6 sau mai multi ganglioni;
pNx: adenopatia regionalǎ nu poate fi demonstratǎ
pN0: fǎrǎ metastaze ganglionare
pN1: metastaze in ganglionii axilari homolaterali
pN1a: micrometastaze, niciuna peste 0.2 cm
pN1b: metastaze peste 0.2 cm
pN1bi: metastaze in 1-3 ganglioni oricare peste 0.2 cm si toate sub 2 cm in diametru maxim
pN1bii: metastaze in peste 4 ganglioni oricare peste 0.2 cm si toate sub 2 cm in diametru maxim
pN1biii: invazie extracapsularǎ a unui ganglion sub 2 cm in diametrul maxim
pN1biv: ganglion metastazat de cel putin 2 cm in diametrul maxim
PN2: ganglionii axilari homolaterali invadati fixati
pN3: metastaze in ganglionii mamari interni homolaterali
pM- categoriile pM corespund categoriei M
5.4. Clasificarea dupǎ gradul de diferentiere histopatologicǎ
Gx - gradul de diferentiere nu poate fi stabilit
G1 - bine diferentiat
G2 - moderat diferentiat
G3 - slab diferentiat
G4 - nediferentiat (5)
5.5. Stadializarea
Pentru a simplifica clasificatea TNM au fost descrise 5 stadii:
Stadiul 0 sau carcinom in situ este un cancer localizat, neinvaziv care nu s-a rǎspandit mai departe de sistemul ductal al sanului, nu a invadat tesutul normal inconjurator. 15-20% din cancerele de san detectate la o examinare clinicǎ sunt in stadiul 0. Exista 2 tipuri de carcinom in situ (LCIS si DCIS) si boala Paget.
Carcinomul lobular in situ indicǎ un risc ridicat pentru dezvoltarea cancerului de san. Multi clinicieni nu considerǎ acest stadiu ca fiind malign si deseori descoperǎ LCIS din intamplare cu ocazia unor biopsii sau investigatii de altǎ naturǎ asupra sanului. Desi microscopia carcinomului lobular in situ este asemǎnǎtoare celei a cancerului de san, comportamentul este diferit. LCIS este doar un marker care indicǎ un risc crescut de a dezvolta cancer de san. Totusi, in caz de istoric familial relevant pentru cancerul de san, se poate executa o mastectomie bilateralǎ simplǎ. Majoritatea pacientilor cu LCIS sunt monitorizati prin examen clinic al sanului o datǎ la 4 luni si mamografie o datǎ pe an; aditional unii pacienti pot primi tamoxifen pentru a preveni dezvoltarea spre cancer de san.
Carcinomul ductal in situ: celulele canceroase sunt prezente in canalele galactofore, dar nu s-au rǎspandit incǎ in tesutul gras inconjurǎtor sau in nodulii limfatici. DCIS poate fi diagnosticat prin biopsie sau poate fi detectat prin mamografie, in 80% din cazuri apǎrand ca niste mici calcifieri. Rar poate lua aspectul unei mase tumorale cu calcifieri (15%) sau si mai rar ca o masa tumoralǎ fǎrǎ calcifieri (5%). Tratamentul DCIS constǎ in terapia de conservare a sanului: lobectomie urmatǎ de radioterapie sau mastectomie.
Boala Paget este o formǎ rarǎ de cancer, care incepe in canalele galactofore si se extinde la tegument, la mamelon si areola mamarǎ. Tegumentul poate prezenta cruste, tumefiere si secretii. Prognosticul este mai bun dacǎ modificǎrile areolei sunt singurele semne ale bolii si nu existǎ noduli palpabili.
Stadiul I: cancerul primar este de aproximativ 2 cm sau mai putin in diametru si nu s-a rǎspandit la nodulii limfatici
Stadiul II are 2 subdiviziuni IIA si IIB
Stadiul IIA: tumora primarǎ are intre 2 si 5 cm in diametru, dar nu s-a rǎspandit la nodulii limfatici
Stadiul IIB: tumora primarǎ are intre 2 si 5 cm in diametru si s-a rǎspandit la nodulii limfatici axilari de aceeasi parte; sau tumora primarǎ este mai mare de 5 cm in diametru, dar nu s-a rǎspandit la nodulii limfatici
Stadiul III defineste cancerul invaziv si e divizat in douǎ subcategorii IIIA si IIIB
Stadiul IIIA: tumora mǎsoarǎ mai mult de 5 cm in diametru si nodulii limfatici sunt fixati intre ei sau de tesutul inconjurǎtor
Stadiul IIIB: tumora poate avea orice dimensiune si s-a rǎspandit la tegument, peretele toracic sau nodulii limfatici mamari interni; aici intrǎ si cancerul inflamator
Cancerul inflamator - sanul este inflamat (edem si tumefactie prezente) cu modificarea tegumentului cauzatǎ de rǎspandirea celulelor tumorale in cǎile limfatice. Cancerul inflamator se aflǎ la granita dintre afectǎrile benigne (mastita) si inflamatia malignǎ. In cazuri rare, cancerul inflamator se poate rǎspandi foarte rapid si in alte pǎrti ale organismului.
Stadiul IV: cancerul invaziv , tumora s-a extins in afara sanului, axilar, la nodulii limfatici mamari interni, supraclaviculari, plǎman, ficat, oase si creier.(63)
|
Stadiul |
Clasificarea TNM |
|
Stadiu 0: |
cancer in situ - Tis, N0, M0 |
|
Stadiu I: |
T1, N0, M0 |
|
Stadiu IIa: |
T0-1, N1, M0, sau T2, N0, M0 |
|
Stadiu IIb: |
T2, N1, M0, sau T3, N0, M0 |
|
Stadiu IIIa: |
T0-2, N2, M0, sau T3, N1-2, M0 |
|
Stadiu IIIb: |
T4, N (orice), M0, sau T(orice), N3, M0 |
|
Stadiu IV: |
T(orice), N(orice), M1 |
5.6 Stadializǎri aditionale
In stadializarea cancerului de san se mai folosesc si termeni ca: timpuriu, tardiv si avansat.
Stadiul timpuriu cuprinde stadiile 0, I si II.
Stadiul tardiv cuprinde stadiile II in care sunt implicati mai multi noduli limfatici si stadiul III (IIIA si IIIB).
Stadiul avansat cuprinde stadiul IV.
Cu cat stadiul este mai mic, cu atat sansele de supravietuire sunt mai mari.
| Contact |- ia legatura cu noi -| | |
| Adauga document |- pune-ti documente online -| | |
| Termeni & conditii de utilizare |- politica de cookies si de confidentialitate -| | |
| Copyright © |- 2025 - Toate drepturile rezervate -| |
|
|
|||
|
|||
|
|||
Analize pe aceeasi tema | |||
|
| |||
|
|||
|
|
|||








